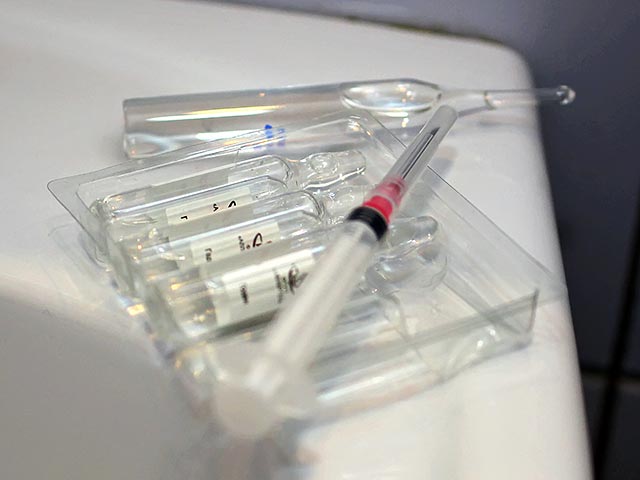
В России сотни тысяч доз вакцин не могут попасть в поликлиники из-за застопорившегося процесса сертификации: с ноября ФГБУ "Научный центр экспертизы средств медицинского применения" (НЦЭСМП) не работает после проверки Росаккредитацией. Чиновники рекомендуют производителям обращаться в другие центры, однако газета "Коммерсант" со ссылкой на представителей фармконцернов сообщает, что на деле в лабораториях нет необходимого оборудования. Производители вакцин заявляют, что если ситуация не разрешится, возможен всплеск детских заболеваний, "вплоть до эпидемии".
По данным издания, сертификацию не могут пройти вакцины против пневмонии, менингита, гепатита А для взрослых и детей, а также комплексные вакцины для ослабленных детей "Пентаксим" и "Инфанрикс Гекса".
НЦЭСМП отстранили от проверок из-за недопустимого, по мнению Росаккредитации, упрощения процесса: там проводились не все пробы, принимая сертификаты независимых европейских компаний, так как не было нужного оборудования. В Минздраве сообщили, что центр решил проводить испытания образцов всех поступающих на сертификацию партий препаратов и подал заявку на расширение области аккредитации. Но до ее одобрения деятельность в этой области приостановлена.
Производитель "Инфанрикс Гекса" концерн GSK обращает внимание на то, что от недостатка вакцины пострадают "наиболее уязвимые к инфекциям люди, в частности дети первых лет жизни". Как разъясняет "Коммерсант", эта вакцина, а также "Пентаксим" производства компании "Санофи Пастер", используются как альтернатива входящей в Нацкалендарь прививок АКДС - их рекомендуют детям со сниженным иммунитетом из-за более щадящего компонента, защищающего от коклюша.
- В этом году Россия может остаться без новых импортных лекарств
В московском консультативно-диагностическом центре по специфической иммунопрофилактике, куда направляют для прививок детей с ослабленным иммунитетом, эти вакцины уже закончились. В "Санофи Пастер" заявили, что если ситуация не изменится, "возможен всплеск заболеваемости у ослабленных детей вплоть до эпидемии".
Представитель "Санофи Пастер" Виктория Еремина сообщила РБК, что проблемы с сертификацией затронули не только "Пентаксим", но и еще четыре вакцины, которые производит компания, в частности "Акт Хиб" от гемофилии. При этом партии, которые не могут получить сертификаты, могли бы удовлетворить потребности 396 тысяч человек, подчеркнули в компании.
Проблемы с пополнением фонда зарубежных комбинированных вакцин РБК подтвердили несколько педиатров и представителей ведущих медицинских государственных центров столицы. По их данным, не хватает вакцин, в частности, в детском Центре диагностики и лечения им. Н.А. Семашко, в Московском НИИ эпидемиологии и микробиологии им. Г.Н. Габричевского, в частном медицинском центре "СМ-Клиника".
Росаккредитация: дефицит вакцин возник давно
В Росаккредитации РБК заявили, что дефицит вакцин возник давно и не связан с приостановкой деятельности НЦЭСМП. Сертификацию препаратов может осуществлять не только ФГБУ НЦЭСМП, "а все органы по сертификации, в области аккредитации которых имеются иммунобиологические препараты", цитирует слова представителей ведомства "Коммерсант". По данным реестра Росаккредитации, таких органов в России пять.
Однако представители фармкомпаний заявили, что сразу после запрета деятельности НЦЭСМП связались со всеми другими лабораториями, и ни в одной из них не хватает оборудования. Этот факт, напомним, и стал причиной того, что НЦЭСМП запросил дополнительной аккредитации. В Минздраве говорят, что там сейчас активно устанавливают необходимое оборудование.
Представитель GSK заявил РБК, что компания рассматривает все законные инструменты для того, чтобы получить сертификаты на свою продукцию. Однако переход в другой орган по сертификации предполагает задержку с поставкой вакцин на рынок.
Кроме того, нет открытого реестра организаций, которые вправе сертифицировать именно комбинированные вакцины, которые требуют подготовки особой нормативной документации, отметил источник.